近日,我院作物病原真菌功能基因組學(xué)研究團(tuán)隊(duì)劉慧泉教授課題組在《Nature Communications》上在線發(fā)表了題為“Unveiling the A-to-I mRNA editing machinery and its regulation and evolution in fungi”的研究論文,揭示了真菌中A-to-I mRNA編輯的酶復(fù)合體,并明確了其起源、進(jìn)化和調(diào)控機(jī)制。該研究為真菌病害防控和基因編輯工具開發(fā)提供了重要的新思路。

A-to-I mRNA編輯是一種關(guān)鍵的遺傳信息修飾機(jī)制,它能夠在mRNA分子中將腺苷(A)轉(zhuǎn)變?yōu)榧≤眨↖)。由于肌苷(I)在化學(xué)結(jié)構(gòu)上與鳥苷(G)相似,因此在蛋白質(zhì)翻譯過程中,肌苷(I)會被當(dāng)作鳥苷(G)來識別和使用,從而可能導(dǎo)致編碼的蛋白序列發(fā)生變化。過去,A-to-I mRNA編輯主要在動物中被研究和報(bào)道,但劉慧泉團(tuán)隊(duì)在2016年首次在真菌中發(fā)現(xiàn)了這一現(xiàn)象,并證明它在小麥赤霉病菌等真菌的有性生殖和適應(yīng)性進(jìn)化中起著至關(guān)重要的作用。在動物中,A-to-I mRNA編輯是由ADAR酶催化的,但真菌中并不存在ADAR的同源基因,這使得真菌中A-to-I mRNA編輯的發(fā)生機(jī)制成為一個科學(xué)謎題。劉慧泉團(tuán)隊(duì)經(jīng)過近8年的深入研究,終于揭開了真菌A-to-I mRNA編輯的發(fā)生機(jī)制。主要研究發(fā)現(xiàn):
真菌中A-to-I mRNA編輯由Tad2-Tad3-Ame1酶復(fù)合體催化。Tad2-Tad3異源二聚體是真核生物中保守的tRNA特異的腺苷脫氨酶,主要負(fù)責(zé)tRNA反密碼子環(huán)上第34位的A-to-I編輯。真菌中特異性進(jìn)化出的一種蛋白Ame1打破了這一底物識別的限制,使得Tad2-Tad3-Ame1三元復(fù)合體能夠識別和編輯mRNA。
真菌中A-to-I mRNA編輯特異性發(fā)生在有性生殖階段的原因。mRNA編輯激活因子Ame1僅在有性生殖階段誘導(dǎo)表達(dá),這是A-to-I mRNA編輯特異性發(fā)生在有性生殖階段的直接原因。此外,轉(zhuǎn)錄水平和翻譯后水平的調(diào)控對編輯酶復(fù)合體在有性生殖階段的活性也起到關(guān)鍵作用。A-to-I mRNA編輯雖然對真菌有性生殖有利,但當(dāng)在無性階段人工表達(dá)Ame1激活A(yù)-to-I mRNA編輯后會對小麥赤霉病菌生長和侵染不利。因此,A-to-I mRNA編輯特異性發(fā)生在有性生殖階段,不僅避免了由編輯自身帶來的生存與生殖之間的權(quán)衡問題,還能化解因基因拮抗多效性造成的生存與生殖權(quán)衡,從而促進(jìn)真菌在生存與生殖兩方面的最優(yōu)化。
真菌中A-to-I mRNA編輯機(jī)制的起源和進(jìn)化。mRNA編輯激活因子Ame1的同源基因在真菌界中普遍存在,并在不同真菌世系中經(jīng)歷了多次復(fù)制和水平基因轉(zhuǎn)移事件。特別是在糞殼菌綱和錘舌菌綱真菌的最近共同祖先上,發(fā)生了一次基因復(fù)制事件。這一復(fù)制事件產(chǎn)生的一個拷貝在糞殼菌綱真菌的進(jìn)化過程中,通過快速變異,獲得了與Tad3互作的能力,最終進(jìn)化成了mRNA編輯激活因子Ame1。
真菌A-to-I mRNA編輯系統(tǒng)具有廣闊的應(yīng)用前景。研究表明,真菌的A-to-I mRNA編輯系統(tǒng)具有廣泛的適用性,可用于基因編輯工具的設(shè)計(jì)和開發(fā),特別是針對基因治療,用于修復(fù)人類的遺傳疾病。此外,A-to-I mRNA編輯酶復(fù)合體將是控制真菌病害的優(yōu)良靶標(biāo)。
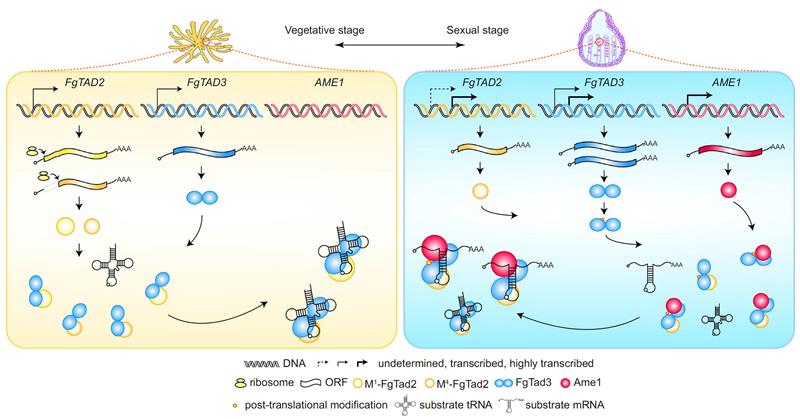
真菌中A-to-I mRNA編輯酶復(fù)合體的工作原理和調(diào)控機(jī)制
我院劉慧泉教授為論文通訊作者,博士研究生馮嬋婧(現(xiàn)為博士后)、辛凱蕓(現(xiàn)為博士后)、杜雁飛、鄒靖雯為論文共同第一作者。康振生院士、王曉杰教授、江聰研究員和王秦虎副教授以及生命學(xué)院黃偉偉副教授對論文研究也做出了重要貢獻(xiàn)。該研究得到國家重點(diǎn)研發(fā)計(jì)劃、國家自然科學(xué)基金、博士后創(chuàng)新人才支持計(jì)劃等項(xiàng)目資助。
全文鏈接:
https://www.nature.com/articles/s41467-024-48336-8?utm_campaign=related_content&utm_source=HEALTH&utm_medium=communities
課題組應(yīng)邀在Springer Nature Research Communities上分享了該科學(xué)發(fā)現(xiàn):Unveiling the Mystery of Fungal RNA Editing Machinery: A Story of Unexpected Discoveries (https://communities.springernature.com/posts/unveiling-the-mystery-of-fungal-rna-editing-machinery-a-story-of-unexpected-discoveries)
編輯:劉小鳳
審核:郭 軍


