近日,我院作物疫霉功能基因研究與利用研究團(tuán)隊(duì)在期刊《Nature Communications》上在線發(fā)表了題為“PsAF5 functions as an essential adapter for PsPHB2-mediated mitophagy under ROS stress in Phytophthora sojae ”的研究論文。該研究發(fā)現(xiàn)了含ANK和FYVE結(jié)構(gòu)域的蛋白PsAF5作為線粒體內(nèi)膜自噬受體PsPHB2的配體,通過影響PsPHB2與PsATG8的互作從而參與調(diào)控大豆疫霉響應(yīng)活性氧的線粒體自噬機(jī)制。我院已畢業(yè)博士李文浩、在讀博士朱宏偉和陳金珠為論文共同第一作者,苗建強(qiáng)副研究員和劉西莉教授為論文共同通訊作者。

寄主植物響應(yīng)病原菌侵染后能在其細(xì)胞質(zhì)外體空間產(chǎn)生活性氧(Reactive oxygen species,ROS),是植物先天免疫系統(tǒng)的重要防御反應(yīng),而線粒體作為細(xì)胞物質(zhì)和能量的代謝中心,不僅是細(xì)胞內(nèi)活性氧的主要來源,也是活性氧損傷的主要靶向?qū)ο蟆D壳埃≡?yīng)蛋白如何抑制寄主ROS的產(chǎn)生已被廣泛研究,然而,關(guān)于植物病原卵菌在侵染過程中如何增加ROS耐受能力并維持線粒體穩(wěn)態(tài)的問題尚不清楚。
該研究首先通過生物信息學(xué)分析,發(fā)現(xiàn)大豆疫霉中存在10個(gè)同時(shí)含有ANK和FYVE結(jié)構(gòu)域 AFs 基因,并對這類基因進(jìn)行了敲除與表型分析。發(fā)現(xiàn) PsAF5 敲除轉(zhuǎn)化子對H2O2敏感性增加,致病力顯著降低,推測PsAF5是大豆疫霉響應(yīng)ROS脅迫的重要因子。進(jìn)一步研究發(fā)現(xiàn),活性氧處理下PsAF5與PsATG8的互作和共定位增強(qiáng),而且 PsAF5的敲除能夠阻止活性氧處理和線粒體自噬誘導(dǎo)劑處理?xiàng)l件下的線粒體自噬發(fā)生。蛋白互作及系列驗(yàn)證試驗(yàn)表明,PsAF5通過ANK結(jié)構(gòu)域與線粒體內(nèi)膜蛋白PsPHB2互作從而被招募到受損線粒體,且線粒體在活性氧壓力下受損導(dǎo)致的PsPHB2外露是其與PsAF5互作的必要條件。綜上,PsAF5作為PsATG8與PsPHB2互作的“橋梁”,將PsATG8招募到活性氧壓力下受損的線粒體,啟動線粒體自噬途徑。
該研究首次發(fā)現(xiàn)一個(gè)新的配體蛋白PsAF5,在PsPHB2招募PsATG8中發(fā)揮“橋梁”的作用。由于AFs蛋白在不同真核生物中均存在,因此作者推測PHB2-AF5-ATG8蛋白復(fù)合體及其功能模式在其他真核生物中可能保守存在。研究結(jié)果豐富了人們對于真核生物受體介導(dǎo)型線粒體自噬的認(rèn)識,同時(shí)也為新型藥劑分子靶標(biāo)的發(fā)掘提供了理論基礎(chǔ)。
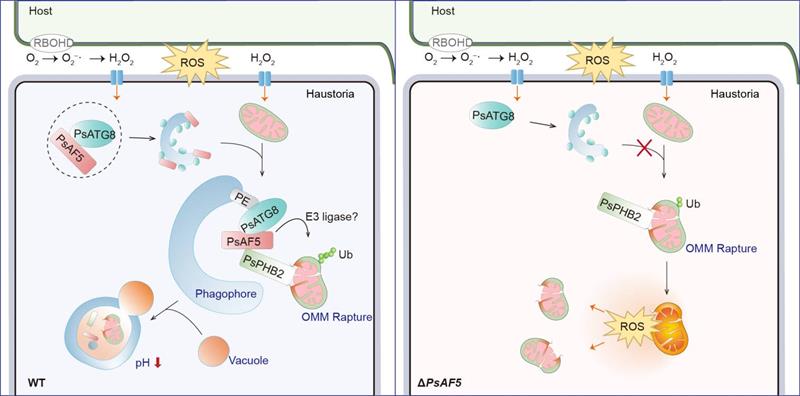
PsAF5作為“配體”在活性氧誘導(dǎo)的線粒體自噬中的作用
該研究工作得到了國家自然科學(xué)基金和陜西省科技創(chuàng)新團(tuán)隊(duì)等項(xiàng)目的資助。作物抗逆與高效生產(chǎn)全國重點(diǎn)實(shí)驗(yàn)室實(shí)驗(yàn)平臺為研究工作完成提供了技術(shù)支持。
原文鏈接:https://www.nature.com/articles/s41467-024-46290-z
編輯:劉小鳳
審核:郭 軍


